ASPSCR1::TFE3 orchestrates the angiogenic program of alveolar soft part sarcoma
Tanaka, M., Chuaychob, S., Homme, M., Yamazaki Y., Lyu R., Yamashita K., Ae K., Matsumoto S., Kumegawa K.,
Maruyama R., Qu W., Miyagi Y., Yokokawa R. and Nakamura T.
Nat Commun 14, 1957 (2023). https://doi.org/10.1038/s41467-023-37049-z
Copyright: © 2023 by the authors. This article is an open access article distributed under the terms and conditions of the Creative Commons Attribution (CC BY) license (https:// creativecommons.org/licenses/by/ 4.0/).
ASPSにおけるASPSCR1::TFE3の役割と血管新生活性の調節メカニズムの解明
背景
腫瘍の血管新生はがんの悪性進行と遠隔転移において最も重要なプロセスのひとつです。
胞巣状軟部肉腫(ASPS)はまれで、一般的に若年成人に発生し、高い転移性を持つことから予後不良の腫瘍です。ASPSの腫瘍は血管豊富な胞巣状構造が特徴で、それが頻繁な転移を引き起こす原因とされています。ASPSの血管形成調整機能の解明が治療方法開発に役に立つことが期待されています。
本研究の成果
モデルマウスやエピゲノム編集技術でASPSの原因とされている融合転写因子ASPSCR1::TFE3の機能とその標的遺伝子を明らかにし、ASPSの血管形成メカニズムを解明しました。
本研究におけるPrimeSurface®の使用方法
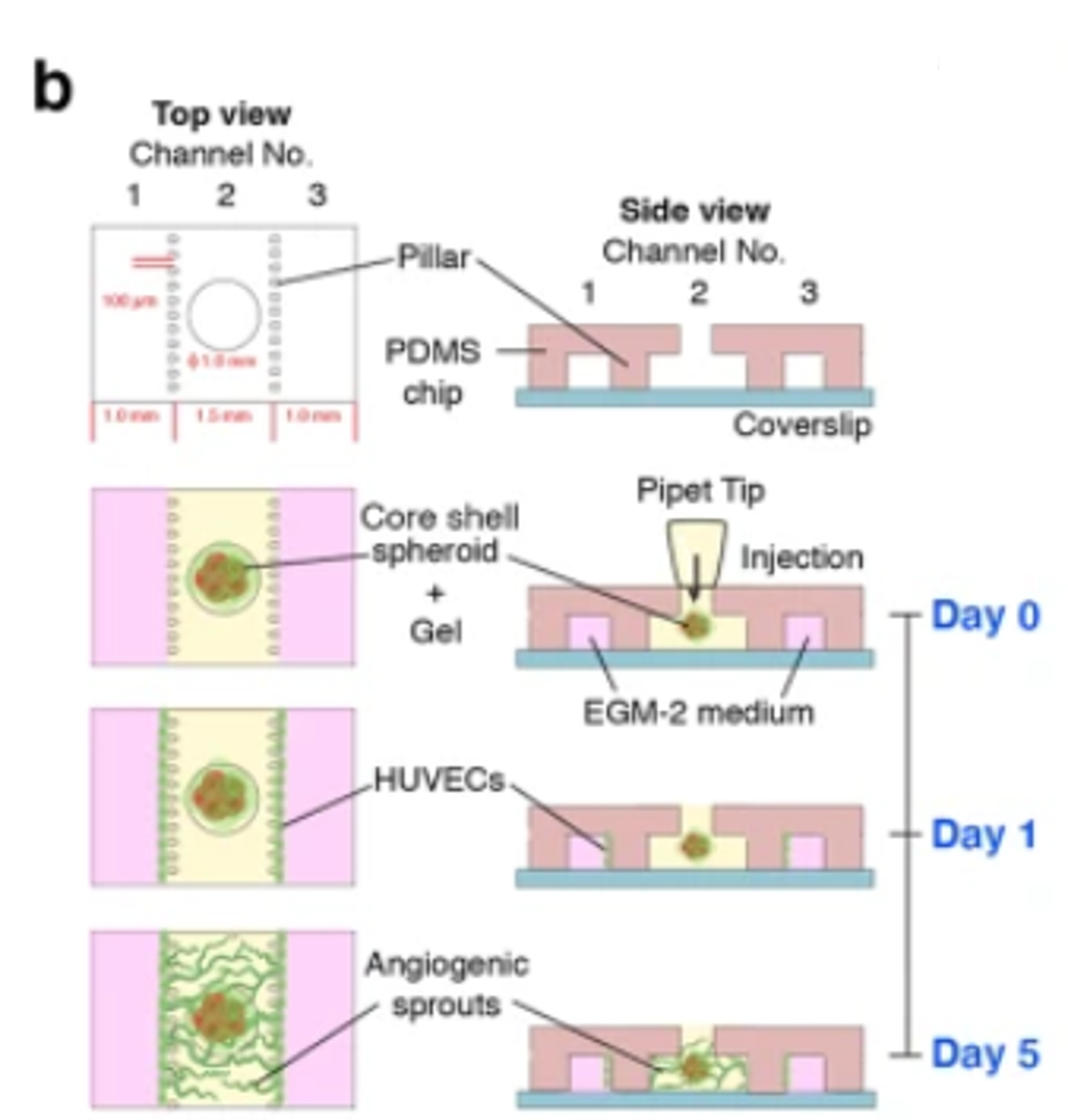
PrimeSurface®で作製されたスフェロイドとorgan-on-a-chipシステムでin vivoでのASPSの複雑な血管構造を再現:
| 1. | 5.0 x 104 cells/mLのASPS cellsをPrimeSurface 96Uプレートで2日間培養し、 |
|---|---|
| 2. | 7.5 x 104 cells/mLのPericytesを添加しASPS cellsの凝集塊の外周に凝集させ、 |
| 3. | 作製された腫瘍スフェロイドを図示のようにマイクロ流路を刻んだチップに供した(Day0)。 |
| 4. | 流路にHUVEC細胞を播種し(Day1)、スフェロイドと共培養を行い、4日後に血管形成を評価した(Day5)。 |
【結果】
ASPSとPericytes細胞から作製された腫瘍スフェロイドとHUVECとの共培養により、腫瘍スフェロイドに向かって血管形成が観察された。
| 品番 | 品名 | ウェル数 | 色 | ウェル底形状 | ウェル 容量 |
包装 | 参考単価 (円) |
参考ケース 価格 (円) |
|---|---|---|---|---|---|---|---|---|
| MS-9096U | PrimeSurface® 96Uプレート |
96 | 透明 | U底 | 300 μ | 1/包, 20/ケース | 1,730 | 34,600 |
注記
- 放射線滅菌済
- 保管温度: 室温, 有効期限: 製造後2年
- 参考価格(本体価格・税抜)
トピックス すべてを見る
- 2025/01/28 製品情報 Cell-able®製品販売終了のお知らせ
- 2025/01/27 メルマガ S-BIO Insight『毛包誘導形成にPrimeSurfaceを活用!最新研究の成果をご報告』
- 2025/01/20 製品情報 新製品「EZGlyco® mAb-N kit with APTS」発売のお知らせ
- 2025/01/20 製品情報 ステムフル®の新規アプリケーションデータ「細胞回収用低吸着遠沈管ステムフル®のF-hiSIEC™(ヒトiPS細胞由来腸管上皮細胞)回収における比較試験」を追加しました
- 2024/12/25 メルマガ S-BIO Insight『ヒト母乳の糖鎖分析による新たな発見』を配信しました
- 2024/12/13 製品情報 PrimeSurafce®の新規アプリケーションデータ「PrimeSurface®プレート96Vを使用した階層スフェロイド型BBBモデル」を追加しました