製品紹介
生物学的活性を持つ1-84PTHのみを特異的に測定する試薬です。従来のintact PTH測定系では抗体のアミノ酸認識部位がN末端側の1-34領域と広範囲であったのに対し、Whole PTH測定系ではN末端の端を特異的に認識する抗体を用いているため、真に生理活性のある1-84PTHのみを測定することが可能となっています。
【製造販売元】富士レビオ株式会社
【販売元】住友ベークライト株式会社
- ※ ルミパルスプレスト® whole PTH「SBBIO」は、免疫発光測定装置ルミパルスL2400またはルミパルス Presto®Ⅱ(富士レビオ株式会社)用の副甲状腺ホルモン(1-84PTH:Whole PTH)測定試薬です。
- ※ CLEIA:chemiluminescent enzyme immunoassay(化学発光酵素免疫測定法)
- ※ 写真左:ルミパルス プレスト® whole PTH「SBBIO」
写真右:ルミパルス プレスト® whole PTH「SBBIO」キャリブレータ
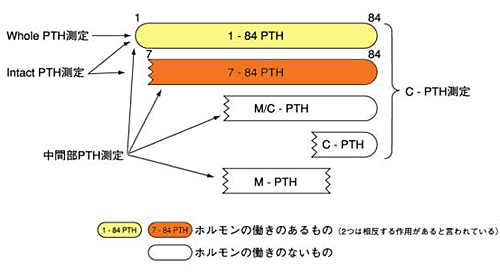
PTH(parathyroid hormone:副甲状腺ホルモン)は、副甲状腺から分泌され、血中カルシウム濃度を上昇させるように働くホルモンです。84個のアミノ酸からなる分子量約9,500のホルモンで、アミノ基がついている側をN末端、カルボキシル基がついている側をC末端といい、生理作用はN末端側に存在するとされています。
PTHは、大部分が84個のアミノ酸からなるインタクトPTHとして副甲状腺から分泌されますが、一部はN末端あるいはC末端などを含むPTHフラグメントの形で分泌されています。一方、末梢血においては、副甲状腺からの分泌に加えてインタクトPTHが肝臓や腎臓で代謝されるために、生物活性を持たない中間部およびC端フラグメントなど多様なフラグメントが存在しています。
ルミパルス プレスト® whole PTH「SBBIO」は、生物学的活性を持つ1-84PTHのみを特異的に測定する試薬です。従来のintact PTH測定系では抗体のアミノ酸認識部位がN末端側の1-34領域と広範囲であったのに対し、Whole PTH測定系ではN末端の端を特異的に認識する抗体を用いているため、真に生理活性のある1-84PTHのみを測定することが可能となっています。
用途
体外診断用医薬品
先行
化学発光免疫測定法(CLEIA)による血漿中又は血清中全長型副甲状腺ホルモン(whole PTH, 1-84PTH)の測定
使用方法
キットの操作方法
本試薬は、免疫発光測定装置ルミパルス Presto®Ⅱ(富士レビオ株式会社)用の副甲状腺ホルモン(1-84PTH:Whole PTH)測定試薬です。測定装置の操作に関する詳細は、ルミパルス Presto®Ⅱの取扱説明書をご参照下さい。
試薬の調製法
-
①抗体結合粒子
冷蔵庫から出してそのまま使用します。
試薬を装置にセットする場合は、試薬を泡立てないようにゆるやかに20回以上転倒混和して、ボトル底部に沈殿している粒子を再懸濁してください。 -
②酵素標識抗体
冷蔵庫から出してそのまま使用します。転倒混和はしないでください。
-
③PTHキャリブレータ(別売品)
常温(15~25℃)に戻してから軽く転倒混和して使用します。
デッドボリュームを考慮して、サンプルカップに必要量を滴下します。- キャリブレータ1滴あたりのおよその滴下量は45μLです。滴下量は容器を押す強さや気泡の混入によって変動します。滴下の際に液滴の中に気泡が多量に混入する場合は、残量が僅かですので新しい試薬を使用してください。サンプルカップに泡が残りますとサンプリング不良の原因になる場合があります。
- デッドボリュームは、一例としてルミパルスPresto®Ⅱでサンプルカップをご使用の場合、100μLとなります。
-
④基質液
冷蔵庫から出してそのまま使用します。
- 基質の漏れがないように装置にセットしてください。
- 基質液を装置にセットした後は、基質液交換時まで取外しは避けてください。基質液がアルカリホスファターゼ(ALP)に汚染されますと使用できません。手指が直接基質液に触れた場合は、廃棄してください。
-
⑤洗浄液
ルミパルスPresto®Ⅱの取扱説明書に従い補充してください。洗浄液は装置内において自動的に精製水で10倍に希釈されます。
必要な器具・器材
- ① ルミパルスPresto®Ⅱ(富士レビオ株式会社)
- ② LPコントロール・PTH(別売品)
精度管理用試料として、LPコントロール・PTHを推奨いたします。
使用に際しては、LPコントロール・PTHの取扱説明書を参照してください。 - ③ ルミパルスPresto用サンプリングチップ
- ④ ルミパルスPresto用キュベット
- ⑤ ルミパルスPresto用アッセイキャップA、アッセイキャップB
- ⑥ マイクロピペット、サンプルカップ
測定法
- ① ルミパルス Presto®Ⅱの取扱説明書を参照し、検体および測定に必要な試薬を所定の位置にセットしてください。
- ② 抗体結合粒子、酵素標識抗体のボトルキャップを静かに外し、口元に付着している試薬は清潔な紙等でふき取ります。ボトル内に泡立ちが残っているときはしばらく放置して泡立ちがないことを確認するか、または清潔な綿棒等を用いて取除きます。
- ③ アッセイキャップを取付けます。取付け方は、下記の(8)アッセイキャップの取付け方の欄をご参照ください。
- ④ ボトルのバーコードが濡れていたり、汚れていたりした場合は、ふき取ってからセットしてください。
- ⑤ 試薬を試薬保冷庫内のカローセルにセットします。抗体結合粒子はカローセルAに、酵素標識抗体はカローセルBに、それぞれセットします。試薬は、カローセルの空いている場所のどこにでもセットすることができます。また、装置からカローセルを取出して試薬をセットすることもできます。ボトルをセットした後はカローセルを静かに装置の所定位置へ戻します。
- ⑥ 基質液は蓋を取外し、基質保冷庫へセットします。
- ⑦ 洗浄液は測定システムの取扱説明書に従い補充します。
- ⑧ アッセイキャップの取付け方
アッセイキャップは装置にセットした試薬の蒸発や汚染を防ぐために使用します。新しいボトルを装置にセットする際には、新しいアッセイキャップを取付けてからご使用ください。取付けない場合は、測定結果の信頼性は保証できません。取付けた後は、アッセイキャップに液が付着しないように、装置にセットするまでボトルを傾けないよう注意して取扱ってください。・アッセイキャップAの取付け方
アッセイキャップAは、抗体結合粒子ボトルの口元に乗せ、回しながら止まるまで締めて取付けます。アッセイキャップAの外側を上から静かに押し(図1)、内部のゴムスリットが開口することを確かめます(図2)。
スリットに膜が形成されている場合はアッセイキャップAを一旦取外し、清潔な紙等で裏のゴム表面の液体をふき取り、再びボトルに取付けます。
ゴムスリットがきちんと開口しないときや、アッセイキャップAが円滑に動かないときは、再度外側を押して確認します。改善がみられないときは新しいアッセイキャップAに交換してください。・アッセイキャップBの取付け方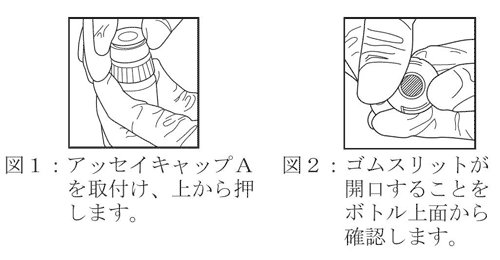
アッセイキャップBは、酵素標識抗体ボトルに使用します。取付ける際は、まずボトルキャップを外し代わりにアッセイキャップBをボトル口元に乗せます。図3のように、ボトル上部の鍔(つば)とアッセイキャップB下部の突起が、ぶつかって止まるまで回しながら締めて取付けます。 図3の★の位置を上から指で押して、蓋が開くことを確かめます(図4)。 ボトルの口に膜が形成されている場合は清潔な紙等で蓋のゴム表面に付着した液体をふき取ってください。 アッセイキャップBが締まらないときや、押しても蓋が円滑に動かないときは一旦取外し、再度取付けます。改善がみられないときは、新しいアッセイキャップBに交換してください。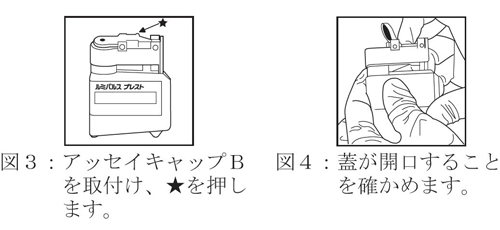
- ⑨ 試薬の他に、測定に必要なサンプリングチップおよびキュベットが十分量投入されていること、精製水タンク、洗浄液タンク、濃縮洗剤タンクの残量が十分であることを確認します。
- ⑩ 分析の受付操作を行います。
- ⑪ 検体を検体分析用のラックにセットし、装置の所定位置にセットします。精度管理分析の場合は精度管理分析用のラックを、キャリブレーション分析の場合はキャリブレーション分析用のラックをそれぞれ使用します。
- ⑫ 外箱記載のデータ入力バーコードには、PTHキャリブレータの使用期限およびロット番号が記録されています。装置付属のバーコードリーダーを用いて読み取ることにより、PTHキャリブレータのロット管理を自動的に行うことができます。
- ⑬ スタートキーを押して測定を開始します。
濃度の算出法
マスターキャリブレーションデータは、酵素標識抗体ボトルの2次元バーコードに記録されています。検体中のPTH濃度は、PTHキャリブレータの発光量をもとに較正された検量線から自動的に算出されます。また複数装置をお使いの場合は1台ごとに検量線を作成してください。
*キャリブレーションは以下の場合に行います。
- 抗体結合粒子、酵素標識抗体、基質液のいずれかが、新しいロットに切り替わった場合。
- キャリブレーションデータを更新後、30日が経過した場合。
上記以外においても必要が生じた場合は、PTHキャリブレータを測定しキャリブレーションデータを更新してください。
※ 検体中のPTH濃度が、5,000pg/mLを超える場合は、0pg/mL PTHキャリブレータを用いて希釈し、再測定してください。なお、希釈は10倍希釈までの範囲で行ってください。
仕様
| 統一商品コード | 品名 | 包装単位 | 貯法 |
|---|---|---|---|
| 713200094 | ルミパルス プレスト® whole PTH「SBBIO」 | 200回用 | 2~10℃ |
測定原理
本試薬は1ステップサンドイッチ法に基づいたCLEIA(chemiluminescent enzyme immunoassay:化学発光酵素免疫測定法)による副甲状腺ホルモン(1-84PTH:Whole PTH)測定試薬です。
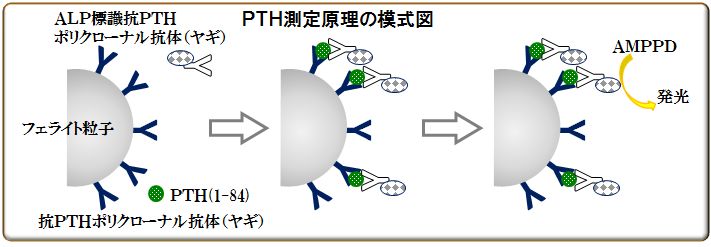
- ① 抗C末端PTH(39-84)ポリクローナル抗体(ヤギ)を固定したフェライト粒子と検体中のPTH(1-84),アルカリフォスファターゼ(ALP)標識抗N末端PTHポリクローナル抗体(ヤギ)を反応させる。
- ② 磁石を用いてB/F分離を行って未反応のALP標識抗N末端PTHポリクローナル抗体(ヤギ)を除去する。
- ③ AMPPDを加えて酵素反応を行い、その後AMPPD分解に伴う発光量をルミノメーターで測定し、予め作成した検量線より検体中PTH(1-84)濃度を算出する。
AMPPD:化学発光基質
3-(2’-spiroadamantane)-4-methoxy-4-(3’’-phosphoryloxy)phenyl-1,2-dioxetane disodium salt
貯蔵方法・有効期間
貯法
2~10℃に保存してください。
有効期間
製造後1年(有効期限はキット外箱に表示)
別売品
ルミパルス プレスト® whole PTH「SBBIO」キャリブレータ
| 構成試薬品 | 分量 |
|---|---|
| 1. PTH 0pg/mL | 3.0mL×1 (液状) |
| 2. PTH 5000pg/mL | 1.50mL×1 (液状) |
【販売元】住友ベークライト株式会社
LPコントロール・PTH
| 構成試薬品 | 分量 |
|---|---|
| PTHコントロール | 2濃度×2/各3.0mL |
【販売元】富士レビオ株式会社
保険収載内容
D008 内分泌学的検査「29」副甲状腺ホルモン(PTH):161点
(2024年6月1日改定)
よくあるご質問
Q1. PTHの生体内でどのような機能を果たしていますか?
A1. |
副甲状腺ホルモン(Parathyroid Hormone: PTH)は副甲状腺(上皮小体)より分泌されるホルモンで、 84個のアミノ酸より構成されており、カルシウム及びリンの代謝調節を行なっています。 PTHの標的器官は主として骨と腎臓で、血中のカルシウムの低下により副甲状腺から分泌され、骨吸収亢進による カルシウム動員および腎細尿管でのカルシウム再吸収を促進して血中カルシウムの上昇をもたらし、 腎臓における1,25水酸化ビタミンD3の合成を促進して小腸でのカルシウム吸収を高める働きをしています。 |
|---|
Q2. Whole PTHとは何ですか?
A2. |
「Whole」は、「全長型の」という意味で使われています。即ち、1~84番目までのアミノ酸が すべて揃ったものがWhole PTHです。 |
|---|
Q3. Intact PTHとの違いは何ですか?
A3. |
「Intact」とは、「そのままの、損なわれていない」という意味ですが、Intact PTH測定法は活性 のある1-84PTH(Whole PTH)と7-84PTHフラグメントの総和となります。 |
|---|
Q4. Whole PTHとIntact PTHの値に相関関係はありますか?
A4. |
一般的には、「Intact PTH」=1.7×「Whole PTH」と言われています。 |
|---|
Q5. Whole PTHの参考基準範囲はどのくらいですか?
A5. |
本品を用いて、健常者169例を対象に、血清及び血漿中のWhole PTH値を測定し、測定値を対数変換で正規化して 求めたところ、平均値は19.2 pg/mL、平均値±1.96標準偏差は8.3~38.7 pg/mLとなりました。 |
|---|
Q6. Whole PTHの管理目標値はどのくらいですか?
A6. |
慢性腎臓病に伴う骨・ミネラル代謝異常の診療ガイドライン(2012)において、透析患者の Whole PTHは35 pg/mL 以上150 pg/mL 以下の範囲に管理することが望ましいと記載されています。 |
|---|
Q7. Whole PTHとIntact PTHを同時に算定することはできますか?
A7. |
同時算定はできません。 |
|---|
Q8. ルミパルスプレストWhole PTH「SBBIO」の測定にはどのような設備が必要ですか?
A8. |
本試薬は、全自動化学発光酵素免疫測定システム(ルミパルスL2400及びルミパルスPrestoⅡ)用試薬です。 なお、本試薬の構成試薬にはキャリブレータ及びコントロールは含まれていません(別売)。 |
|---|
Q9. 検体は血清、血漿のどちらが使えますか?
A9. |
検体には、EDTA血漿、ヘパリン血漿及び血清を用いることができます。 |
|---|
Q10. 検体の安定性は?
A10. |
検体は採取後できるだけ早く測定し、保存する場合は-20℃以下で凍結保存してください。 |
|---|
Q11. 凍結融解は何回まで測定に影響を及ぼしませんか?
A11. |
3回以上凍結融解を繰り返した検体は使用しないでください。 |
|---|
Q12. 検体を取り扱う上で注意すべきことはありますか?
A12. |
PTHはガラスやプラスチック容器に吸着することが知られています。 |
|---|
Q13. キットの測定範囲はどのぐらいですか?
A13. |
4.0~5000 pg/mLです。5000 pg/mLを超える検体は、0 pg/mL PTHキャリブレータで希釈後、測定してください。 |
|---|
Q14. 採血は何mL必要ですか?
A14. |
血清又は血漿として約3mLです。 |
|---|
添付文書
関連資料
 基礎データ集(準備中)
基礎データ集(準備中) SDS(準備中)
SDS(準備中) SDS キャリブレータ(準備中)
SDS キャリブレータ(準備中)
ご利用上の注意事項
住友ベークライト株式会社の製品情報ウェブサイトへアクセスいただきありがとうございます。
製品情報のサイトでは医療関係者の方を対象に体外診断用医薬品等の弊社製品を適正にご使用いただくための情報を提供しております。
このサイトをご利用いただくための注意事項です。必ずお読み下さい。
- 1.国内の医療関係者を対象としており、国外の医療関係者、一般の方に対する情報提供を目的としたものではありません。
- 2.掲載している情報は、体外診断用医薬品等の弊社製品を適正にご使用いただくためのものであり、広告を目的とするものではありません。
- 3.このサイトの内容に関する著作権は、住友ベークライト株式会社またはこのサイトに情報掲載を許諾した
- 4.提供者に帰属しておりますので、無断転載は固くお断りします。
上記以外の「ご利用上の注意」につきましては、ご利用上の注意をご覧下さい。
医療関係者で、かつ上記の注意事項にご同意いただける方のみアクセスしてください。
よろしいですか?